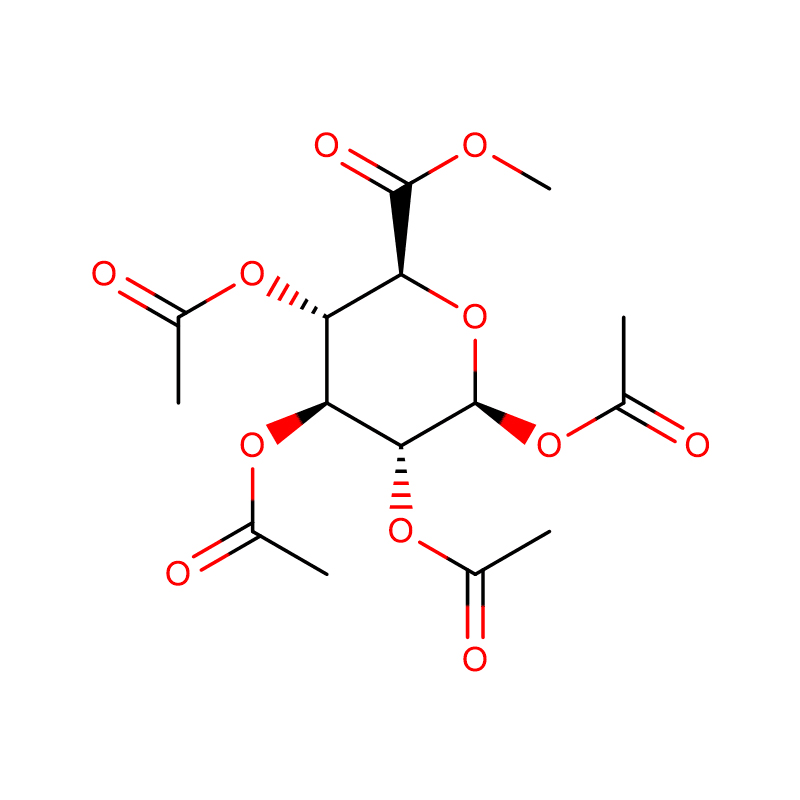
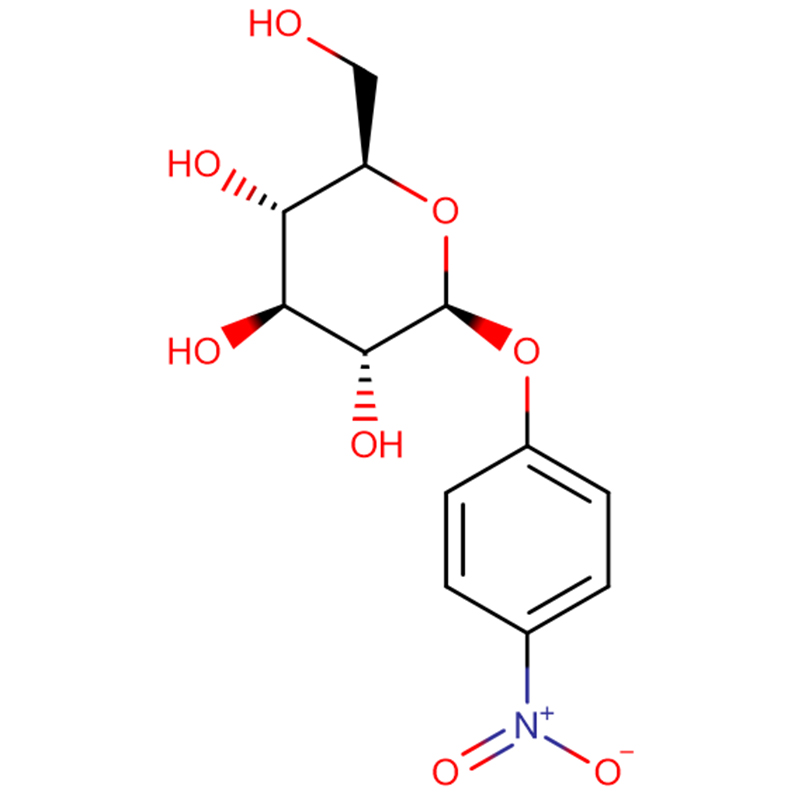
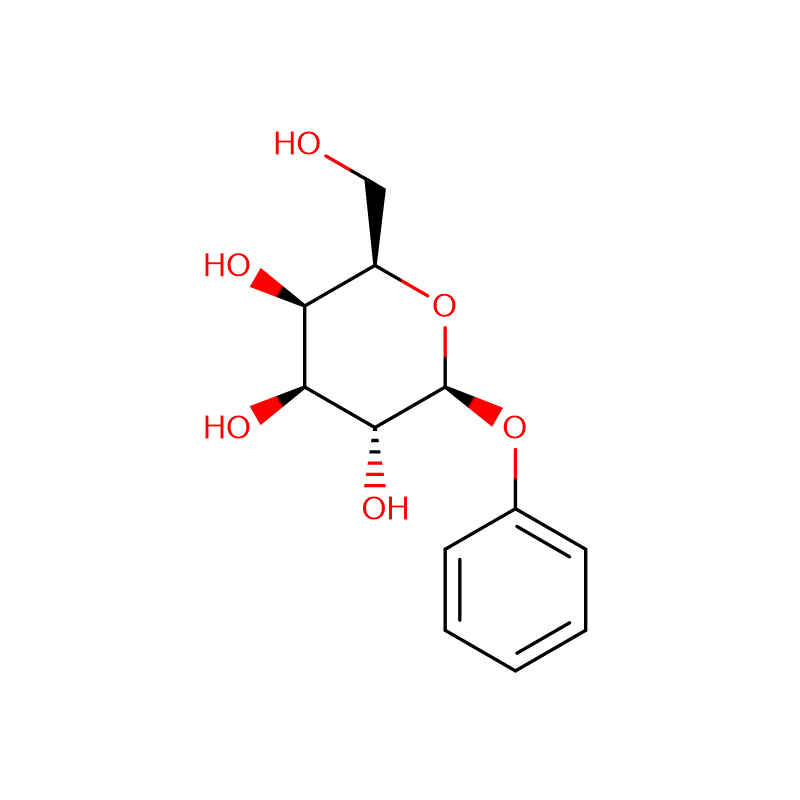
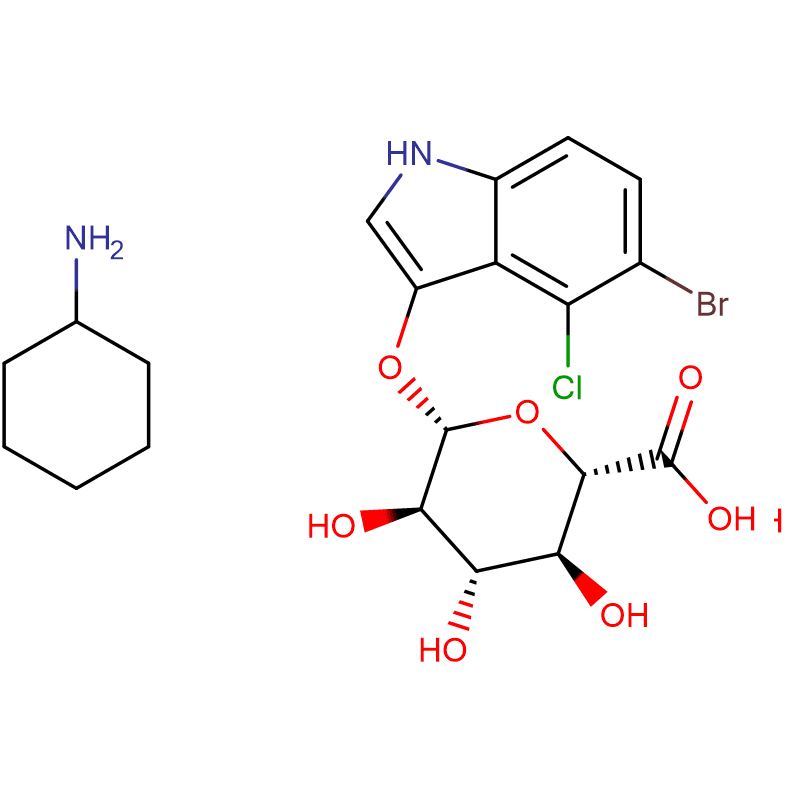
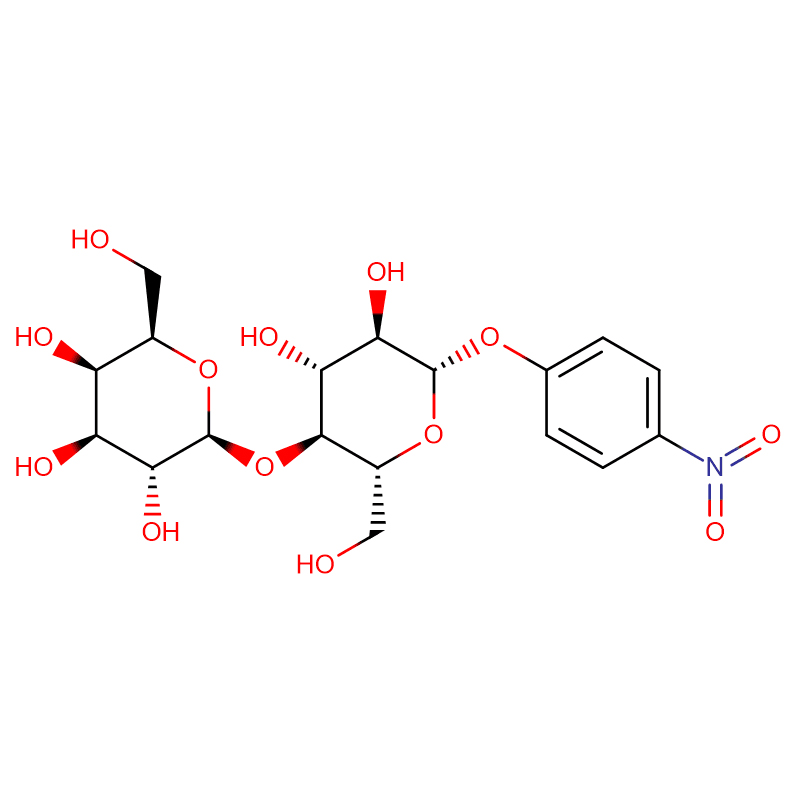
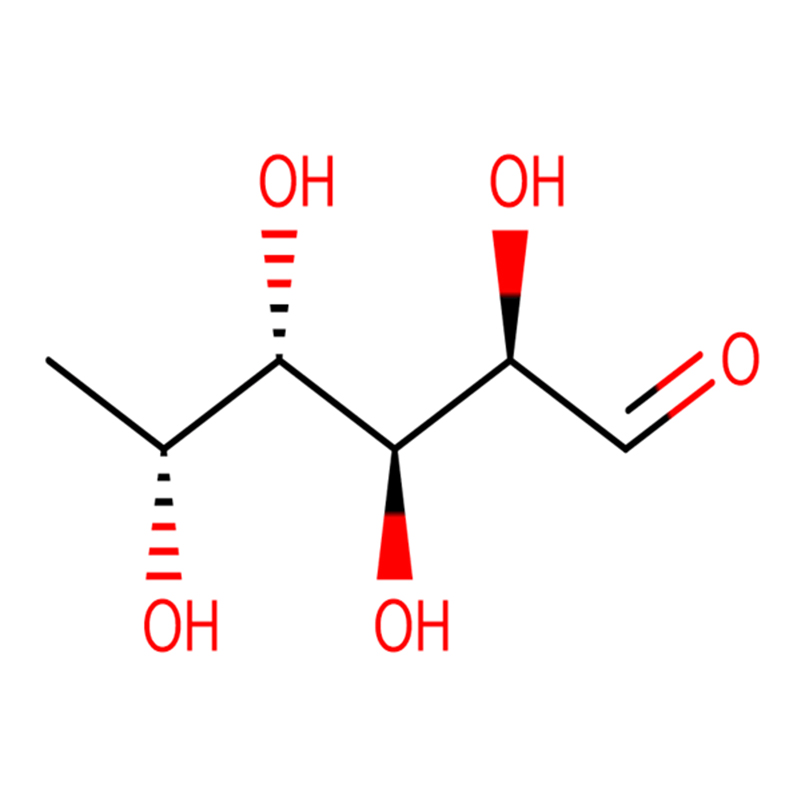
Två isomera bicyklo[4.1.0]heptananaloger av glykosidasinhibitorn galakto-validamin, (1R*,2S,3S,4S,5S,6S*)-5-amino-1-(hydroximetyl)bicyklo[4.1.0]heptan -2,3,4-triol, har syntetiserats i 13 steg från 2,3,4,6-tetra-O-bensyl-D-galaktos.De hämmande aktiviteterna för de två konformationsmässigt begränsade aminerna, och deras motsvarande acetamider, mättes mot kommersiella alfa-galaktosidas-enzymer från kaffebönor och E. coli.Aktiviteten hos enzymet GH27 från glykosylhydrolasfamiljen (kaffeböna) inhiberades kompetitivt av 1R,6S-aminen (7), en bindningsinteraktion som kännetecknades av ett K(i)-värde på 0,541 mikroM.GH36 E. coli alfa-galaktosidas uppvisade en mycket svagare bindningsinteraktion med 1R,6S-aminen (IC(50)= 80 mikroM).Den diastereomera 1S,6R-aminen (9) band svagt till båda galaktosidaserna (kaffeböna, IC(50)= 286 mikroM) och (E. coli, IC(50)=2,46 mM).